 دکتر احمدرضا طاهری بجد
دکتر احمدرضا طاهری بجد
متخصص بیماری های پوست - فلوشیپ پوست کودکان
استاد دانشگاه
شپش سر (Head Lice / Pediculosis capitis)
شپش سر معمولاً از طریق تماس اتفاقی از فردی به فرد دیگر منتقل می شود. اگرچه می تواند ناخوشایند باشد، اما گزینه های درمانی موثری وجود دارد. برای جلوگیری از سرایت شپش به دیگران، یافتن و درمان سریع بسیار مهم است.
سیکل زندگی
شپش سر یک حشره ریز و سفید مایل به خاکستری است. شپشهای ماده معمولاً حدود یک ماه عمر میکنند و روزانه 7 تا 10 تخم (nit) میگذارند. تخم ها به پایه تار مو، نزدیک پوست سر متصل می شوند. تخم ها بعد از حدود هشت روز باز می شوند. تخم ها پس از باز شدن، راحت تر دیده می شوند. از آنجایی که تخم ها محکم به مو چسبیده اند، با رشد مو از پوست سر دور می شوند. شپش سر جهش و پرواز نمی کند و نمی تواند با چسبیدن به حیوانات خانگی از فردی به فرد دیگر سرایت کند. شپش بالغ می تواند تا 55 ساعت بدون میزبان زنده بماند.

اپیدمیولوژی
شپش سر در سرتاسر جهان و در افراد با هر زمینه اجتماعی و اقتصادی رخ می دهد. اغلب کودکان را مبتلا می کند. در یک مطالعه، تقریباً از هر چهار دانشآموز مقطع ابتدایی در ایالات متحده، یک نفر شپش سر داشت. مردان کمتر از زنان مبتلا می شوند، دلایل این امر مشخص نیست، و مطالعات در خصوص تاثیر بلندی مو بر خطر آلودگی، نتایج متناقضی را به همراه داشته است.
انتقال
تصور می شود که تماس مستقیم با موهای فرد مبتلا به شپش (تماس مو به مو) رایج ترین روش انتشار شپش است. میزان تأثیر تماس با اشیاء مورد استفاده افراد مبتلا به شپش، مانند لباس، ملافه، شانه یا برس، در گسترش شپش سر نامشخص و نتایج مطالعات متناقض بودهاست.
علایم بالینی
- اکثر افراد مبتلا به شپش هیچ علامتی ندارند. برخی از افراد احساس خارش یا سوزش پوست در سر، گردن و گوش دارند. این ناشی از واکنش به بزاق شپش است که حشره در هنگام تغذیه به پوست تزریق می کند. البته در یک بیمار بدون آلودگی قبلی، شروع خارش ممکن است تا زمانی که حساسیت پس از چهار تا شش هفته رخ دهد به تعویق بیفتد.
علاوه بر شپش و نیت، بر روی پوست سر، گردن و پشت گوش نیز ممکن است آثار خراشیدگی (excoriations) قابل مشاهده باشد. به ندرت، عفونت استافیلوکوکی ثانویه همراه با بزرگ شدن غدد لنفاوی گردنی یا پسسری رخ می دهد.
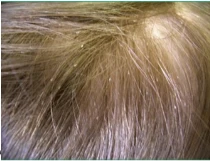
نیت های متعدد روی ساقه مو

پاپول های اگزکوریه روی گوش به همراه نیت روی موها
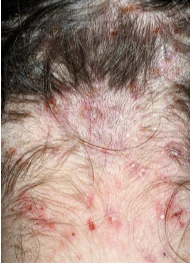
اگزکوریشن و کراستهای متعدد روی گردن
تشخیص
در بیماران مبتلا به خارش پوست سر، به ویژه در کودکان، باید مشکوک به شپش سر بود. پیودرمی (pyoderma) پایدار از جمله زردزخم در اطراف گردن یا گوش نیز باید باعث ارزیابی از نظر شپش سر شود.
شپش سر با معاینه پوست سر و مو تشخیص داده می شود. تشخیص با مشاهده شپش زنده تایید می شود. شانه کردن مرتب و کامل موهای خیس یا خشک با یک شانه دندانه ریز (دندانههای شانه به فاصله 0.2 میلی متر از هم) آلودگی شپش فعال را بهتر از بررسی بصری مو و پوست سر به تنهایی تشخیص می دهد. براساس یک مطالعه، شانه کردن مرطوب حساس ترین روش تشخیصی است.
برای انجام شانه کردن مرطوب (wet combing)، ابتدا از یک روان کننده (lubricant) مانند نرم کننده مو به موها استفاده می شود و سپس مراحل زیر (که برای روش شانه کردن خشک نیز استفاده می شود) صورت میگیرد:
-موها برس یا شانه میشوند تا گرههای مو از بین بروند.
-یک شانه دندانه ظریف (که "شانه های تخم" یا nit combs نیز خوانده میشود) در نزدیکی تاج سر قرار داده می شود تا زمانی که به آرامی پوست سر را لمس کند، پس از آن محکم به سمت پایین کشیده می شود و پس از هر ضربه از نظر وجود شپش بررسی می شود.
-کل سر حداقل دو بار به طور سیستماتیک شانه می شود.
نیتها اغلب راحتتر از شپشهای بالغ یافت میشوند. برخلاف فلسهای سبورئیک، قالبهای مو (hair casts) و بقایای اسپری مو، نیتها محکم به ساقه مو چسبیدهاند و به سختی از جای خود خارج میشوند.
زمانی که پزشک یا پرستار سر را زیر لامپ مخصوص معاینه میکند، نیتها درخشش به رنگ آبی کمرنگ دارند. دیدن حشرهها نسبت به نیتها دشوارتر است زیرا می توانند حرکت کنند و از دید پنهان شوند.
با این حال، یافتن نیتها بدون حشره، آلودگی فعال را تایید نمی کند. نیتها می توانند پس از درمان موفقیت آمیز، برای ماه ها همچنان وجود داشته باشند. از آنجایی که شپش ها در قاعده ساقه مو تخم می گذارند، آلودگی فعال با یافتن تعداد زیادی از نیتها در یک چهارم اینچ (6.5 میلی متر) از پوست سر مطرح می شود. نیتهای دورتر از پوست سر تقریبا همیشه غیرقابل زندگی هستند. با این حال، حتی این معیار منجر به تشخیص بیش از حد (overdiagnosis) می شود.
پیدا کردن شپش می تواند برای کودکان و والدین ناراحت کننده باشد، اما مهم است که موارد زیر را به آنان گوشزد نمایید:
- شپش سر نشانه کثیف یا بیمار بودن نیست.
- با درمان مناسب می توانید از شر شپش سر خلاص شوید.
- هیچ مشکل جدی یا طولانی مدت سلامتی مرتبط با شپش سر وجود ندارد.
تشخیص افتراقی
نیتها باید از قالبهای مو (Hair casts) که همچنین به عنوان نیتهای کاذب (pseudonits) شناخته میشوند، افتراق داده شود. کستهای مو غلافهای کراتینی و لولهای سفید تا زرد 2 تا 7 میلیمتری هستند که ساقههای مو را احاطه کردهاند. ممکن است ایدیوپاتیک (اولیه) باشد یا ممکن است در ارتباط با بیماری پوست سر مانند درماتیت سبورئیک یا پسوریازیس رخ دهد. بر خلاف نیت، کستهای مو به راحتی در امتداد ساقه مو می لغزند.

پوسته های سفید و قابل جابجا کردن اطراف ساقه مو ( کست مو )
درمان
درمان پدیکولوز سر توصیه میشود. شپشکش (pediculicide)های موضعی رایج ترین درمان های اولیه هستند. برداشتن دستی شپش (شانه کردن مرطوب) گاهی اوقات به عنوان یک درمان جایگزین شپشکش موضعی استفاده می شود. درمان خوراکی گاهی اوقات برای آلودگی های مقاوم به درمان مورد نیاز است.
صرف نظر از درمان انتخاب شده، وجود شپش زنده باید قبل از درمان تایید شود. بیماران مبتلا به نیت در بیش از 6.5 میلی متری از پوست سر و بدون شپش بالغ قابل تشخیص، احتمالاً عفونت فعال ندارند. لذا این بیماران نیازی به درمان ندارند.
بسیاری از بیمارانی که دارای نیت به فاصله کمتر از 6.5 میلی متری از پوست سر هستند و شپش بالغ قابل تشخیص ندارند نیز آلودگی فعال ندارند. رویکردهای پزشکان به این بیماران متفاوت است. در حالی که برخی از پزشکان درمان را بر اساس احتمال از دست دادن مشاهده شپش زنده حین معاینه تجویز میکنند، برخی دیگر از نظر بالینی بیماران را ازنظر امکان بروز علائم آلودگی فعال دنبال می کنند تا از درمان غیرضروری اجتناب کنند.
درمان خط اول
پدیکولوسیدهای موضعی متعددی بهعنوان درمان های خط اول برای پدیکولوزیس سر پذیرفته شده است. شانه کردن مرطوب یک مداخله جایگزین است که عمدتاً برای شیرخواران کم سنوسال و بیمارانی که ترجیح می دهند از شپشکش اجتناب نکنند استفاده می شود.
مهم است که دستورالعمل ها به دقت اجرا گردد تا درمان موثر واقع گردد. بایستی اعضای خانواده و تماس های نزدیک همزمان معاینه و در صورت نیاز درمان شوند. روش های درمانی بدون نیاز به نسخه (OTC) برای کودکان بالای دو سال در دسترس است.
داروهای موضعی حشرهکش (Insecticides):
نمونههای داروهای موضعی موثر عبارتند از:
Permethrin
Malathion
Benzyl alcohol
Spinosad
Topical ivermectin
قابل ذکر است Topical lindane به دلیل نگرانی هایی در خصوص ایمنی دارو، به عنوان خط اول درمان توصیه نمی شود.
از بین لیست فوق در حال حاضر پرمترین در ایران موجود و روتین است. لوسیون پرمترین 1% درمان قابل تحمل و ارزانی است که سابقه طولانی استفاده برای پدیکولوز سر دارد و انتخاب ارجح برای درمان اولیه در مناطقی هست که مقاومت به این دارو ثابت نشده است. پرمترین می تواند برای بیماران با سن بالای 2 ماه استفاده شود. سمیت بسیار اندکی برای انسان دارد و عارضه مهم آن تحریک پوستی است.
در بیمارانی که به درمان پرمترین با نحوه استفاده مناسب پاسخ نداده اند، باید سایر روشهای درمانی را بکار گرفت.
نحوه استفاده:
فقط یک داروی موضعی باید در هر دفعه استفاده شود. دستورالعمل های شرکت سازنده بایستی به دقت اجرا گردد. مبانی اصلی درمانی عبارتند از:
-باید قبل از استفاده از داروهای موضعی، از استفاده از نرم کننده مو یا محصولات ترکیبی شامپو و نرم کننده خودداری شود. این فراوردهها ممکن است تاثیر درمان را کاهش دهد. دارو باید روی موی خشک مالیده شود.
- شستشوی شپشکشهای موضعی باید بهجای حمام روی سینک انجام شود، تا در معرض پوست قرار گرفتن دارو محدود گردد.
- برای به حداقل رساندن اتساع عروقی و احتمال جذب سیستمیک، شستشو با آب گرم نسبت به آب داغ ترجیح داده می شود.
اکثر ترکیبات موضعی بعد از 10 دقیقه شستشو داده می شوند (به استثنای مالاتیون: 12-8 ساعت). پس از درمان باید لباس تمیز پوشیده شود. حداقل یک تا دو روز پس از استفاده از دارو، موها نباید شسته شوند.
استفاده از یک "شانه تخم" برای حذف شپش و نیت پس از درمان ممکن است به کاهش خطر ابتلا به عفونت مجدد کمک کند. شانه زدن را می توان هر دو تا سه روز به مدت دو تا سه هفته انجام داد.
چه زمانی دوباره درمان تکرار شود
ممکن است چند شپش زنده 8 تا 12 ساعت پس از استفاده از حشرهکش دیده شوند و اگر کندتر از قبل از درمان حرکت میکنند، نیازی به استفاده مجدد دارو نیست. با این حال، اگر شپش مانند قبل از درمان فعال باشد، درمان ممکن است موثر نباشد و روش درمانی دیگری باید مدنظر گیرد.
اکثر شپشکش ها باید دو بار استفاده شوند تا موثر باشند. درمان مجدد هفت تا نه روز پس از اولین درمان صورت میگیرد؛ به این دلیل که برخی از شپش ها می توانند در اولین درمان زنده بمانند.

شانه زدن مرطوب (Wet-combing)
شانه کردن مرطوب راهی برای از بین بردن شپش از روی مو با شانه زدن دقیق و مکرر است. این یک گزینه خوب برای درمان کودکان بسیار کم سن و یا در موارد امتناع از درمان موضعی است. با این حال، شانه کردن مرطوب زمان بر است و باید چندین بار در یک دوره چند هفته ای تکرار شود.
موها بایستی خیس شده و یک روان کننده (lubricant) مانند نرم کننده مو، سرکه یا روغن زیتون به آن اضافه شود. از یک شانه دندانه ریز برای شانه کردن موها استفاده گردد. بسته به طول و ضخامت مو، هر جلسه شانه زدن باید 15 تا 30 دقیقه طول بکشد. بعد از مشاهده هر شپش بزرگ و بالغی، شانه زدن هر سه تا چهار روز یکبار به مدت دو هفته ادامه یابد.
پدیکولوز مقاوم
شایع ترین علل شکست درمان عدم پایبندی به درمان و تماس مداوم با سایر افراد آلوده است. مقاومت در برابر بعضی درمانهای موضعی خاص ممکن است در برخی مکانها مشکل اصلی باشد.
اگر بیمار به یک دوره درمانی مناسب با یک شپشکش موضعی پاسخ ندهد و آلودگی مجدد مطرح نباشد، تغییر به یک درمان موضعی جایگزین که با مقاومت موضعی همراه نباشد، گام معمولی بعدی است. ایورمکتین خوراکی یک گزینه درمانی برای بیمارانی است که درمان موضعی به شکست انجامیدهاست.
ایورمکتین خوراکی
ایورمکتین (200-400 میکروگرم بر کیلوگرم، تکرار بعد از 8 روز) عموما در صورت استفاده برای پدیکولوزیس سر به خوبی تحمل می شود. برای زنان باردار یا کودکان با وزن کمتر از 15 کیلوگرم توصیه نمی شود، زیرا ایمنی دارو در این جمعیت ها ثابت نشده است.
سایر روشها
انواع دیگری از درمانها برای پدیکولوزیس سر مؤثر گزارش شدهاند، مانند دایمتیکون، لیندان، تری متوپریم-سولفامتوکسازول، و انواع روش های فیزیکی. استفاده روتین از بسیاری از این مداخلات به دلیل دادههای اثربخشی محدود یا نگرانیهای ایمنی توصیه نمیشود.
دایمتیکون
یک ماده غیر آفتکش و مبتنی بر سیلیکون است که با پوشاندن شپش ها و مختل کردن توانایی آنها در مدیریت آب عمل می کند. مدت قرارگرفتن آن روی پوست سر در مطالعات مختلف از 15 دقیقه تا 8 ساعت بودهاست.
لیندان
شامپو لیندان 1% برای درمان پدیکولوز سر توصیه نمی شود زیرا با عوارض جانبی عصبی نادر و مقاومت گسترده همراه است. بر اساس توصیه FDA لیندان فقط باید به عنوان یک درمان خط دوم در بیمارانی استفاده شود که نمی توانند سایر درمان ها را برای درمان گال یا شپش تحمل کنند یا درمان شکست خورده است. لیندان در بیماران مبتلا به اختلالات پوستی که ممکن است منجر به افزایش جذب سیستمیک شود (مانند درماتیت آتوپیک، پسوریازیس) منع مصرف دارد.
در صورت استفاده از لیندان موارد زیر توصیه میشود:
-حداقل مقدار ممکن استفاده شود.
-بیشتر از 4 دقیقه روی پوست اسکالپ نباشد.
-فقط یک بار استفاده شود و از درمان مجدد اجتناب گردد.
-هنگام استعمال از دستکش مناسب استفاده شده و بلافاصله بعد از اتمام کار دستها کامل شسته شوند.
کوتریموکسازول
درمان ترکیبی تری متوپریم-سولفامتوکسازول (10 میلی گرم بر کیلوگرم در روز تری متوپریم در دو دوز منقسم) به مدت ده روز به همراه پرمترین موضعی فقط در موارد مقاوم باید در نظر گرفته شود.
روشهای فیزیکی
برداشتن مو (Hair removal): تراشیدن مو به طور غیرمستند (anecdotally) به عنوان روشی برای ریشهکنی شپش سر گزارش شده است. اما، مطالعاتی برای ارزیابی این روش درمانی انجام نشده است، و این روش ممکن است از نظر روانی برای برخی از بیماران ناراحت کننده باشد.
درمانهایی که توصیه نمی شوند
مطالعات لوسیون ها و سایر مواد (روغن زیتون، کره، سس مایونز، وازلین) را بررسی کرده اند که با هدف خفه کردن شپش ها روی سر مالیده شده تا خشک شوند. با این حال، شپش به سختی خفه می شود. شانه زدن احتمالاً در این حد موثر بوده و بهعلاوه روش تمیزتری است.
جلوگیری از انتشار شپش سر
بزرگسالان و کودکانی که با فرد مبتلا به شپش زندگی می کنند باید از نظر شپش معاینه و در صورت نیاز (وجود شپش یا نیت در فاصله کمتر از 1 سانتی متری پوست سر) درمان شوند. هرکسی که در همان تخت میخوابد باید تحت درمان پروفیلاکتیک قرار گیرد، حتی اگر تخم شپش پیدا نشود.
لباسها، ملافهها و حولههایی که طی 48 ساعت قبل از درمان استفاده شدهاند، باید در آب داغ شسته و یا در خشککن برقی در حالت داغ خشک شوند. دما باید حداقل به 130 درجه فارنهایت (معادل 55 درجه سانتیگراد) برسد. خشک شویی نیز موثر است. می توان از جاروبرقی برای تمیز کردن مبلمان، فرش و صندلی ماشین استفاده کرد. اقلامی که قابل شستشو یا جاروبرقی نیستند را می توان به مدت دو هفته داخل کیسه پلاستیکی قرار داد. اقلامی که فرد بیش از دو روز قبل از درمان از آنها استفاده کرده است به احتمال زیاد آلوده نیستند زیرا شپش سر نمی تواند بیش از 48 ساعت دور از بدن زنده بماند. نیازی نیست خانه یا وسایل را با حشره کش اسپری کرد.
خطمشیهای مدرسه درمورد اینکه چه کسی در مدرسه باید در هنگام ابتلا کودک مطلع شود، متفاوت است. تماس یا ملاقات محرمانه با مربی بهداشت مدرسه محل خوبی برای شروع است. اکثر متخصصان بر این باورند که کودکان مبتلا به شپش نیازی به حذف از مدرسه ندارند. کودکان را نباید به دلیل وجود شپش زنده یا تخم از رفتن به مدرسه منع کرد، زیرا شپش ها اغلب هفته ها قبل از تشخیص وجود دارند. علاوه بر این، اکثر کودکان مبتلا به نیت دچار آلودگی فعال نمی شوند. بلکه کودکان مبتلا باید از تماس مستقیم سر با افراد دیگر اجتناب کنند و باید به سرعت تحت درمان قرار گیرند. کلاه و لوازم آرایش مانند برس و شانه نباید مشترک باشد.
کنترل شیوع بیماری در مدارس ممکن است با معاینه معلمان و دانشآموزانی که ممکن است با کودک مبتلا تماس مستقیم داشتهاند و با اختصاص دادن قلابهای دیواری یا قفسههای جداگانه به دانشآموزان برای نگهداری کلاه و کت تسهیل شود. برنامههای آموزشی طراحیشده برای افزایش دانش در مورد پدیکولوزیس سر و روشهای پیشگیری از آلودگی در یک جامعه نیز ممکن است مفید باشد.
منابع:
Uptodate 2022
مبانی درماتولوژی (لوکینگبیل و مارکس) 2019
 سازمان نظام پزشکی ج.ا.ایران
سازمان نظام پزشکی ج.ا.ایران
معاونت آموزشی و پژوهشی
به کوشش :
دکتر بابک پورقلیج

 سازمان نظام پزشکی ج.ا.ایران
سازمان نظام پزشکی ج.ا.ایران


 دکتر حسین علیمددی
دکتر حسین علیمددی


 سازمان نظام پزشکی ج.ا.ایران
سازمان نظام پزشکی ج.ا.ایران
 دکتر حسین علیمددی
دکتر حسین علیمددی

 سازمان نظام پزشکی ج.ا.ایران
سازمان نظام پزشکی ج.ا.ایران
 دکتر احمدرضا طاهری بجد
دکتر احمدرضا طاهری بجد





 سازمان نظام پزشکی ج.ا.ایران
سازمان نظام پزشکی ج.ا.ایران
 دکتر سویل عبدالمحمدیان
دکتر سویل عبدالمحمدیان



 دکتر سید مهدی صمیمی اردستانی
دکتر سید مهدی صمیمی اردستانی 
 دکتر حسن رودگری
دکتر حسن رودگری
 دکتر حسن رودگری
دکتر حسن رودگری

 دکتر حسن رودگری
دکتر حسن رودگری